Your Menurut arrhenius asam adalah zat yang images are ready. Menurut arrhenius asam adalah zat yang are a topic that is being searched for and liked by netizens now. You can Download the Menurut arrhenius asam adalah zat yang files here. Find and Download all free photos.
If you’re looking for menurut arrhenius asam adalah zat yang images information linked to the menurut arrhenius asam adalah zat yang keyword, you have come to the right site. Our site always gives you suggestions for seeing the maximum quality video and picture content, please kindly surf and locate more informative video content and images that fit your interests.
Menurut Arrhenius Asam Adalah Zat Yang. Basa adalah zat yang mengionisasi ion OH dengan melarutkannya dalam larutan air. Menurut Arrhenius asam adalah suatu zat atau molekul yang apabila larut di dalam air akan menghasilkan ion. Teori Asam dan Basa Menurut Arrhenius. Yang larut dalam air akan membentuk ion dan ion sesuai dengan reaksi berikut.
 Pin Di Materi From id.pinterest.com
Pin Di Materi From id.pinterest.com
Menurut Arrhenius basa adalah zatsenyawa yang melepaskan ion OH- ion hidroksida di dalam air. Jika melepaskan 1 buah ion H disebut asam bervalensi 1 jika melepaskan 2 buah ion H disebut asam bervalensi 2 dan seterusnya. Menurut teori Arrhenius asam adalah zat yang di dalam larutan air dapat melepaskan ion H sedangkan basa adalah zat yang di dalam larutan air dapat melepaskan ion OH. Jadi senyawa basa Arrhenius harus mengandung ion OH- di dalam molekulnya. Menurut teori Asam basa Arrhenius asam adalah zat yang dalam air melepaskaan ion H sedangkan basa adalah zat yang dalam air melepaskan ion OH-. LioH NaOH KOH MgOH2 CaOH2 BaOH2 SrOH2 dan lain-lain.
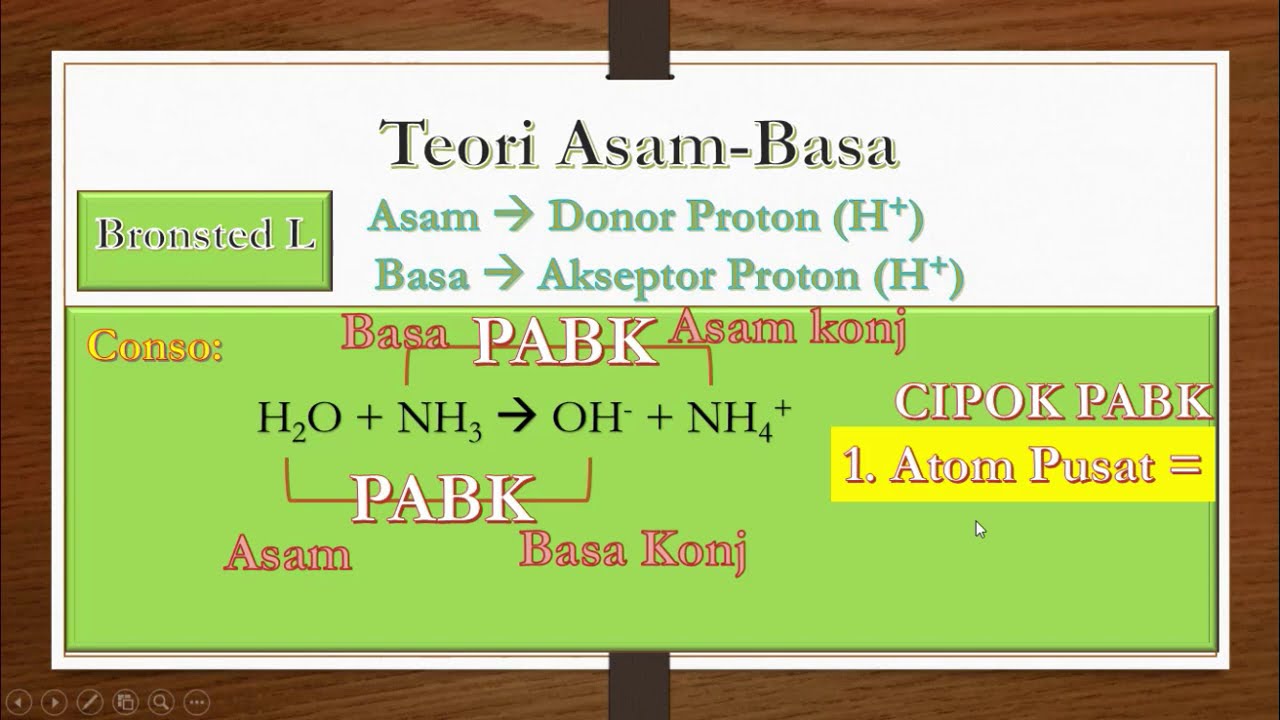
Menurut konsep Bronsted dan Lowry zat yang memiliki kecenderungan untuk menyumbangkan ion H pada zat lain adalah asam.
Menurut Arrhenius asam adalah suatu zat atau molekul yang apabila larut di dalam air akan menghasilkan ion. Ini meningkatkan konsentrasi ion H dalam larutan. Semakin banyak ion OH yang dihasilkan semakin kuat sifat basanya. Menurut teori Arrhenius asam adalah zat yang memberikan ion H saat larut dalam larutan air. Contoh asam adalah. Sedangkan zat yang memiliki kecenderungan untuk menerima ion H dari zat lain adalah basa.
 Source: id.pinterest.com
Source: id.pinterest.com
Seperti yang telah disebutkan pada tulisan Asam Basa Salah satu teori asam basa adalah teori Asam Basa Arrhenius. Menurut teori Asam basa Arrhenius asam adalah zat yang dalam air melepaskaan ion H sedangkan basa adalah zat yang dalam air melepaskan ion OH-. Menurut konsep Bronsted dan Lowry zat yang memiliki kecenderungan untuk menyumbangkan ion H pada zat lain adalah asam. Menurut Arrhenius asam adalah suatu zat atau molekul yang apabila larut di dalam air akan menghasilkan ion. Svante Arrhenius penemu teori asam basa pertama.
 Source: youtube.com
Source: youtube.com
Kemudian ion hidrogen tersebut bergabung dengan molekul air membentuk ion hidronium H3O. Basa adalah zat yang mengionisasi ion OH dengan melarutkannya dalam larutan air. Menurut teori Arrhenius asam adalah zat yang memberikan ion H saat larut dalam larutan air. Menurutnya asam adalah zat yang melepaskan ion H didalam air sedangkan basa adalah zat yang melepaskan ion OH- dalam air. Menurut teori Bronsted Lowry.
 Source: youtube.com
Source: youtube.com
Yang larut dalam air akan membentuk ion dan ion sesuai dengan reaksi berikut. Menurut teori Arrhenius asam adalah zat yang di dalam larutan air dapat melepaskan ion H sedangkan basa adalah zat yang di dalam larutan air dapat melepaskan ion OH. Contoh asam adalah. LioH NaOH KOH MgOH2 CaOH2 BaOH2 SrOH2 dan lain-lain. Kemudian ion hidrogen tersebut bergabung dengan molekul air membentuk ion hidronium H3O.
 Source: br.pinterest.com
Source: br.pinterest.com
Ion OH- adalah pembawa sifat basa pada suatu senyawa. Basa menurut Arrhenius adalah senyawa terlarut dalam air yang menghasilkan ion hidroksida OH. TEORI ASAM BASA DRAFT. Konsentrasi H dan OH dalam larutan dinyatakan dengan pH dan pOH dengan rumus. Menurut teori Arrhenius asam adalah zat yang memberikan ion H saat larut dalam larutan air.
 Source: liveworksheets.com
Source: liveworksheets.com
Ini meningkatkan konsentrasi ion H dalam larutan. Menurut Teori Asam Basa Arrhenius bahwa Asam ialah Zat yang jika didalam Air dapat melepaskan Ion Hidrogen H Ion Ion Hidrogen yang dihasilkan oleh Asam tersebut ketika dilarutkan di dlm Air terikat pada Molekul Molekul Air H2O dlm bentuk Ion Hidronium adalah Ion yang Positif yg dibentuk oleh sebuah Proton Ion Hidrogen pada sebuah Molekul Air. PH log H dan pOH log OH. Contoh senyawa basa Arrhenius. Svante Arrhenius penemu teori asam basa pertama.
 Source: slidetodoc.com
Source: slidetodoc.com
Jumlah ion H yang dihasilkan oleh senyawa asam disebut valensi asam. Ini meningkatkan konsentrasi ion H dalam larutan. Konsentrasi H dan OH dalam larutan dinyatakan dengan pH dan pOH dengan rumus. Menurut teori asam basa Arrhenius basa adalah. Dibawah ini yang tidak benar terkait senyawa asam adalah.
 Source: liveworksheets.com
Source: liveworksheets.com
Menurut teori Asam basa Arrhenius asam adalah zat yang dalam air melepaskaan ion H sedangkan basa adalah zat yang dalam air melepaskan ion OH-. Ion OH- adalah pembawa sifat basa pada suatu senyawa. Seperti yang telah disebutkan pada tulisan Asam Basa Salah satu teori asam basa adalah teori Asam Basa Arrhenius. TEORI ASAM BASA ARRHENIUS. Basa adalah zat yang mengionisasi ion OH dengan melarutkannya dalam larutan air.
 Source: liveworksheets.com
Source: liveworksheets.com
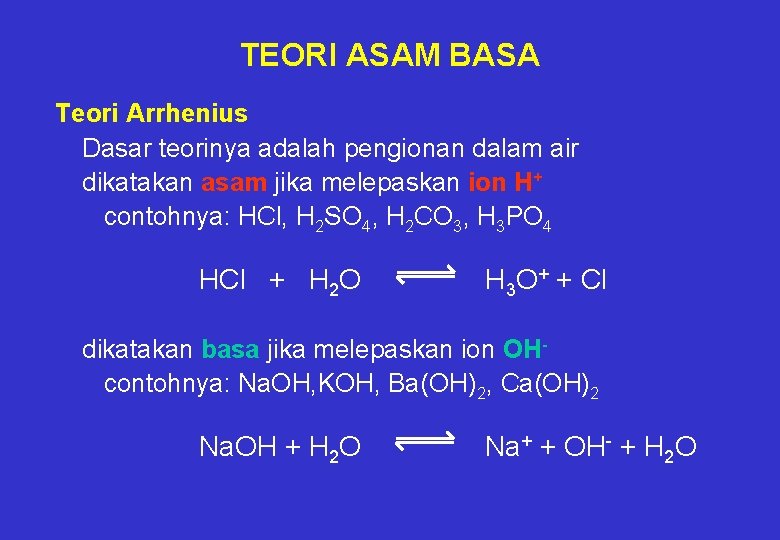
Menurut teori Arrhenius asam adalah zat yang di dalam larutan air dapat melepaskan ion H sedangkan basa adalah zat yang di dalam larutan air dapat melepaskan ion OH. Pada tahun 1884 kimiawan dari Swedia bernama Svante Arrhenius mengusulkan klasifikasi khusus pada senyawa-senyawa yang dinamakan asam dan basa. TEORI ASAM BASA DRAFT. Ion OH- adalah pembawa sifat basa pada suatu senyawa. Svante Arrhenius penemu teori asam basa pertama.
 Source: slidetodoc.com
Source: slidetodoc.com
TEORI ASAM BASA DRAFT. Dibawah ini yang tidak benar terkait senyawa asam adalah. Zat yang dalam air dapat melepaskan ion hidrogen H. Menurut Arrhenius basa adalah suatu zat atau molekul yang akan menghasilkan ion apabila larut didalam air. Menurut konsep Bronsted dan Lowry zat yang memiliki kecenderungan untuk menyumbangkan ion H pada zat lain adalah asam.
 Source: brainly.co.id
Source: brainly.co.id
Semakin banyak ion OH yang dihasilkan semakin kuat sifat basanya. Asam Arrhenius adalah zat yang melepaskan ion hidronium H pada larutan sedangkan basa adalah zat yang melepaskan ion hidroksida OH pada larutan. Menurut Arrhenius asam adalah suatu zat atau molekul yang apabila larut di dalam air akan menghasilkan ion. Adanya ion ini menurut Arrhenius adalah yang bertanggung jawab menyebabkan sifat asam pada suatu senyawa. Yang larut dalam air akan membentuk ion dan ion sesuai dengan reaksi berikut.
 Source: youtube.com
Source: youtube.com
Seperti yang telah disebutkan pada tulisan Asam Basa Salah satu teori asam basa adalah teori Asam Basa Arrhenius. Zat yang dalam air dapat melepaskan ion hidrogen H. Beberapa basa yang dikenal orang dapat dilihat pada tabel berikut. Kemudian ion hidrogen tersebut bergabung dengan molekul air membentuk ion hidronium H3O. Ion OH- adalah pembawa sifat basa pada suatu senyawa.
 Source: coursehero.com
Source: coursehero.com
Asam didefinisikan sebagai zat-zat yang dapat memberikan ion hidrogen H bila dilarutkan dalam air. Menurut teori Asam basa Arrhenius asam adalah zat yang dalam air melepaskaan ion H sedangkan basa adalah zat yang dalam air melepaskan ion OH-. Menurut konsep Bronsted dan Lowry zat yang memiliki kecenderungan untuk menyumbangkan ion H pada zat lain adalah asam. Dibawah ini yang tidak benar terkait senyawa asam adalah. Menurutnya asam adalah zat yang melepaskan ion H didalam air sedangkan basa adalah zat yang melepaskan ion OH- dalam air.
 Source: ar.pinterest.com
Source: ar.pinterest.com
Asam ialah senyawa yang dalam larutannya dapat menghasilkan ion H. TEORI ASAM BASA DRAFT. Teori asam basa Arrhenius hanya dapat menjelaskan sifat asam basa sebatas pelarut air saja karena senyawa asam dan basa umumnya melepaskan ion H atu OH-. Contoh asam adalah. Dibawah ini yang tidak benar terkait senyawa asam adalah.
 Source: youtube.com
Source: youtube.com
Basa dapat menetralisasi asam H dan menghasilkan air H ₂ O. Menurutnya asam adalah zat yang melepaskan ion H didalam air sedangkan basa adalah zat yang melepaskan ion OH- dalam air. Basa menurut Arrhenius adalah senyawa terlarut dalam air yang menghasilkan ion hidroksida OH. Contoh asam adalah. Menurut konsep Bronsted dan Lowry zat yang memiliki kecenderungan untuk menyumbangkan ion H pada zat lain adalah asam.
 Source: utakatikotak.com
Source: utakatikotak.com
Menurutnya asam adalah zat yang melepaskan ion H didalam air sedangkan basa adalah zat yang melepaskan ion OH- dalam air. Pada tahun 1884 kimiawan dari Swedia bernama Svante Arrhenius mengusulkan klasifikasi khusus pada senyawa-senyawa yang dinamakan asam dan basa. Svante Arrhenius penemu teori asam basa pertama. Menurut Arrhenius basa adalah zatsenyawa yang melepaskan ion OH- ion hidroksida di dalam air. Sehingga dapat disimpulkan bahwa.
 Source:
Source:
Menurut teori asam basa Arrhenius basa adalah. Sehingga dapat disimpulkan bahwa. Menurutnya asam adalah zat yang melepaskan ion H didalam air sedangkan basa adalah zat yang melepaskan ion OH- dalam air. Basa adalah zat yang mengionisasi ion OH dengan melarutkannya dalam larutan air. Contoh senyawa basa Arrhenius.
 Source: youtube.com
Source: youtube.com
Svante Arrhenius penemu teori asam basa pertama. LioH NaOH KOH MgOH2 CaOH2 BaOH2 SrOH2 dan lain-lain. Semakin banyak ion OH yang dihasilkan semakin kuat sifat basanya. Jika melepaskan 1 buah ion H disebut asam bervalensi 1 jika melepaskan 2 buah ion H disebut asam bervalensi 2 dan seterusnya. Sehingga dapat disimpulkan bahwa.
 Source:
Source:
Teori asam basa Arrhenius hanya dapat menjelaskan sifat asam basa sebatas pelarut air saja karena senyawa asam dan basa umumnya melepaskan ion H atu OH-. Beberapa basa yang dikenal orang dapat dilihat pada tabel berikut. Menurut Arrhenius basa adalah zatsenyawa yang melepaskan ion OH- ion hidroksida di dalam air. Basa dapat menetralisasi asam H dan menghasilkan air H ₂ O. Basa adalah zat yang mengionisasi ion OH dengan melarutkannya dalam larutan air.
This site is an open community for users to do submittion their favorite wallpapers on the internet, all images or pictures in this website are for personal wallpaper use only, it is stricly prohibited to use this wallpaper for commercial purposes, if you are the author and find this image is shared without your permission, please kindly raise a DMCA report to Us.
If you find this site good, please support us by sharing this posts to your own social media accounts like Facebook, Instagram and so on or you can also save this blog page with the title menurut arrhenius asam adalah zat yang by using Ctrl + D for devices a laptop with a Windows operating system or Command + D for laptops with an Apple operating system. If you use a smartphone, you can also use the drawer menu of the browser you are using. Whether it’s a Windows, Mac, iOS or Android operating system, you will still be able to bookmark this website.





